Batterie da Nobel
di Maria Assunta Navarra, Sergio Brutti e Stefania Panero
Cenni storici
Nella seconda metà del Novecento, la limitata densità di energia delle batterie esistenti spinse la ricerca verso tecnologie di accumulo e materiali alternativi. In particolare, il litio mostrava eccellenti proprietà come materiale elettrodico: è il metallo più leggero (densità 0,53 g/cm-3) ed ha un basso potenziale standard di riduzione (-3,05 Volt vs SHE), che lo rende particolarmente adatto per realizzare batterie ad elevata densità di energia e tensione. Tuttavia, il litio è un metallo reattivo, non può essere esposto ad acqua ed ossigeno. Pertanto, la sua inibizione risultava fondamentale per l’impiego in una batteria.
Ci si concentrò quindi sullo sviluppo di elettroliti non acquosi a conduzione di ioni Li+. I primi studi documentati risalgono al 1958 [1], dove si individuò il propilene carbonato, come solvente alternativo all’acqua, combinato con alogenuri di litio. Gli alchilcarbonati sono, tuttora, i solventi comunemente impiegati nelle batterie al litio.
Ma è solo durante la crisi petrolifera degli anni ‘70 che si fondano i presupposti per il reale sviluppo di tali batterie. L’attenzione fu rivolta all’identificazione dei materiali catodici, in grado di ospitare (intercalare) reversibilmente ioni litio a elevati potenziali di riduzione e buone cinetiche di trasferimento.
Stanley Whittingham fu il primo ad esplorare l’intercalazione elettrochimica del litio nei calcogenuri metallici e a proporne, nel 1973, l’impiego come elettrodi in batteria. Un primo prototipo di batteria fu realizzato nel 1976, costituito da litio metallico (anodo), TiS2 (catodo) e una miscela LiPF6-propilene carbonato (elettrolita), avente una tensione di 2,5 Volt [2]. Tuttavia, la reattività del litio metallico comporta crescita dendritica che può causare corto circuito elettrico con potenziale rischio di incendio/esplosione. Tale problematica, tuttora non risolta, ha frenato lo sviluppo commerciale delle batterie litio-metallico e ha spinto l’attenzione verso soluzioni alternative.
Una configurazione dimostratasi molto promettente fu quella denominata “rocking-chair” (oggi “litio-ione”) in cui entrambi gli elettrodi possono ospitare ioni Li+ [3]. In particolare, la ricerca si spinse verso famiglie di materiali anodici carboniosi. Nel 1985 un gruppo guidato da Akira Yoshino, presso la Asahi Kasei Corporation (Giappone), dimostrò che alcune tipologie di coke di petrolio, dotate di specifici gradi di cristallinità, erano in grado di intercalare Li+ in modo efficiente e reversibile per numerosi cicli di carica-scarica ad un potenziale sufficientemente basso (~ 0,5 Volt rispetto a Li+/Li°) [4].
Nel frattempo, furono investigati materiali catodici innovativi in cui il processo di intercalazione potesse avvenire a tensioni operative più elevate. Nel 1979-1980 John B. Goodenough e i suoi colleghi dell’Università di Oxford proposero LixCoO2 come catodo alternativo [5], in cui gli ioni litio potevano essere ospitati reversibilmente ad una tensione operativa di ~ 4 Volt (vs Li+/Li°).
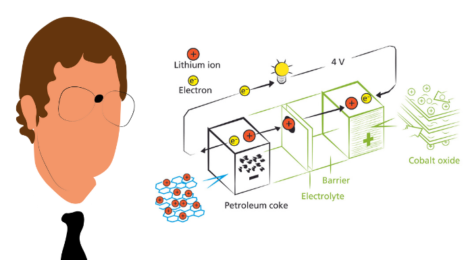
Nel 1991 si pervenne alla prima batteria litio-ione commerciale, realizzata dalla Sony [7]. Essa era costituita da coke di petrolio (anodo), LixCoO2 (catodo) e un elettrolita formato da propilene carbonato (solvente) e LiPF6 (sale). La tensione media era pari a 4 Volt mentre i valori di densità di energia arrivavano a ~ 80 Wh kg-1 (gravimetrica) e ~ 200 Wh L-1 (volumetrica). Rispetto alle altre batterie disponibili sul mercato, quella litio-ione divenne rapidamente molto competitiva e aprì la strada all’imminente rivoluzione dell’elettronica portatile. A meno di qualche ottimizzazione, questa configurazione di batteria è attualmente la più diffusa sul mercato.
Il contributo di Bruno Scrosati
Fin dagli anni ‘70, quando la ricerca sulle batterie litio-ione era appena agli albori, iniziò a distinguersi il contributo di Bruno Scrosati del Dipartimento di Chimica dell’Università di Roma La Sapienza. Risale al dicembre 1979 l’invio dell’articolo, in cui si presentava una cella con due elettrodi ad intercalazione a differente attività di litio [8]. Scrosati, di fatto, dimostrava che l’anodo di litio metallico poteva essere sostituito da un composto ad inserzione, realizzando la prima cella denominata “rocking-chair” e rendendo pratica l’intuizione di Michel Armand sulla possibilità di intercalare ioni litio nei due elettrodi di una batteria [3]. I due scienziati resero quindi possibile la visione di una batteria ricaricabile basata sul trasferimento di ioni litio.
Si deve sempre a Scrosati l’istituzione nel 1982 del più importante convegno tematico sulle batterie al litio, l’International Meeting on Lithium Batteries (IMLB), che oggi conta all’attivo diciannove edizioni di grande successo.
Da allora, Scrosati ha continuato a proporre ed ottimizzare materiali elettrodici ed elettrolitici per batterie. Nel 1997 brevetta “A thin-film lithium polymer battery” [9], a cui segue nel 1998 una pubblicazione Nature sugli elettroliti polimerici [10], che conta più di 2000 citazioni. A 10 anni dal suo pensionamento, Scrosati è ancora tra i chimici più citati al mondo, con 555 lavori censiti nella banca dati Scopus e 56000 citazioni (H-index 94).
Uno sguardo al futuro
La batteria litio-ione è stata una parte fondamentale della rivoluzione dell’elettronica mobile e sta consentendo la transizione dai veicoli a combustibili fossili al trasporto elettrico. Inoltre, l’affermazione definitiva delle fonti rinnovabili dipenderà dalla possibilità di disporre di efficienti sistemi per l’accumulo dell’energia. Dobbiamo quindi ancora assistere alle conseguenze più importanti di questa tecnologia e aspettarci ulteriori avanzamenti. Le scoperte future porteranno senza dubbio a miglioramenti nelle nostre vite e nella sostenibilità del pianeta.
Rispetto alla batteria degli anni ‘90, c’è ampio spazio per l’individuazione di materiali costituenti alternativi, sia elettrodici che elettrolitici, con prestazioni superiori e minore impatto ambientale. Un notevole guadagno, in termini energetici, economici ed ambientali, si ottiene ad esempio dall’uso dello zolfo come materiale catodico, o dall’impiego di anodi ad alligazione basati sul silicio. Allo stesso tempo, la sostituzione degli elettroliti organici, volatili e infiammabili, con materiali conduttori ionici più stabili, quali elettroliti solidi inorganici, polimerici o liquidi ionici, incrementa la sicurezza del dispositivo. Questo filone di ricerca, che riguarda i nuovi materiali per l’accumulo elettrochimico del futuro, è oggi alla base delle attività del gruppo Enam (Electrochemistry and Nanotechnology for Advanced Materials) del Dipartimento di Chimica dell’Università di Roma La Sapienza, che nasce dalla scuola di Bruno Scrosati.
Bibliografia
[1] Harris, W. S.: PhD thesis, University of California, Berkeley, 1958.
[2] Whittingham, M.S.: J. Chem. Soc., Chem. Commun. 1974, 328; Belgian patent n. 819672, 1975; Science 1976, 192, 1126.
[3] Armand, M.B.: NATO Conf. Ser. (VI Mater. Sci.); Murphy, D. W., Broadhead, J., Steele, B.C. H., Eds.; Springer, Boston, MA, 1980, 2, 145.
[4] Yoshino, A. et al: US patent no. 4,668,595, May 26, 1987.
[5] Mizushima, K. et al: Mater. Res. Bull. 1980, 15 (6), 783.
[6] M.A. Navarra et al: La Chimica e l’Industria Online, Anno III, N. 6, Novembre/Dicembre 2019, ISSN 2283-544X
[7] Nishi, Y.: Chem. Rec. 2001, 1, 406.
[8] M. Lazzari and B. Scrosati: J. Electrochem. Soc. 1980 127, 773.
[9] B. Scrosati et al: USA, Air Force, Pat.n. 5,645,960, 07/08/97, Cl, 429-219,000, 1997.
[109] F. Croce et al: Nature, 394 (1998) 456.
Immagine in evidenza: Ritratto di Bruno Scrosati e Adattamento di una rappresentazione della prima batteria litio-ione commercializzata. © Mattia La Torre





















Commenti recenti