Alzheimer, proteina chiave svelata in alta definizione
Gli scienziati della Columbia University hanno studiato il ruolo della proteina tau, legata al morbo di Alzheimer e ad altre malattie neurodegenerative, riportando dettagli strutturali inediti. Per farlo hanno utilizzato due tecnologie da premio Nobel
A quanti miopi è capitato? Non trovate gli occhiali, e, improvvisamente, ciò che avete davanti a voi diventa sfumato, confuso, inaccessibile. Alla fine, dopo svariati tentativi, riuscite a inforcare le lenti: ecco che il mondo riacquisisce i suoi contorni, e voi vedete di nuovo in alta definizione. Studiare la struttura di una proteina può generare una sensazione simile: si apprezzano i margini grossolani della molecola, ma null’altro, rendendo impossibili ulteriori sviluppi di una ricerca. Questa volta un gruppo di scienziati della Columbia University è riuscito a trovare gli occhiali: in uno studio pubblicato su Cell, hanno svelato la struttura della proteina tau, correlata a malattie come il morbo di Alzheimer, con un dettaglio senza precedenti.
Da tempo è noto il ruolo chiave di tau in numerose malattie neurodegenerative, che prendono il nome di taupatie. Rimane tuttavia l’interrogativo di come questa possa convertirsi da una forma funzionale a una tossica. Le proteine, infatti, una volta prodotte all’interno della cellula, acquisiscono una struttura precisa, che ne garantisce il corretto funzionamento. Non sempre ciò accade: a volte si ripiegano in maniera anomala, il che può innescare una reazione a catena che culmina con l’accumulo di proteine in strutture fibrose, caratteristiche delle malattie in cui è alterata la normale funzionalità dei neuroni.
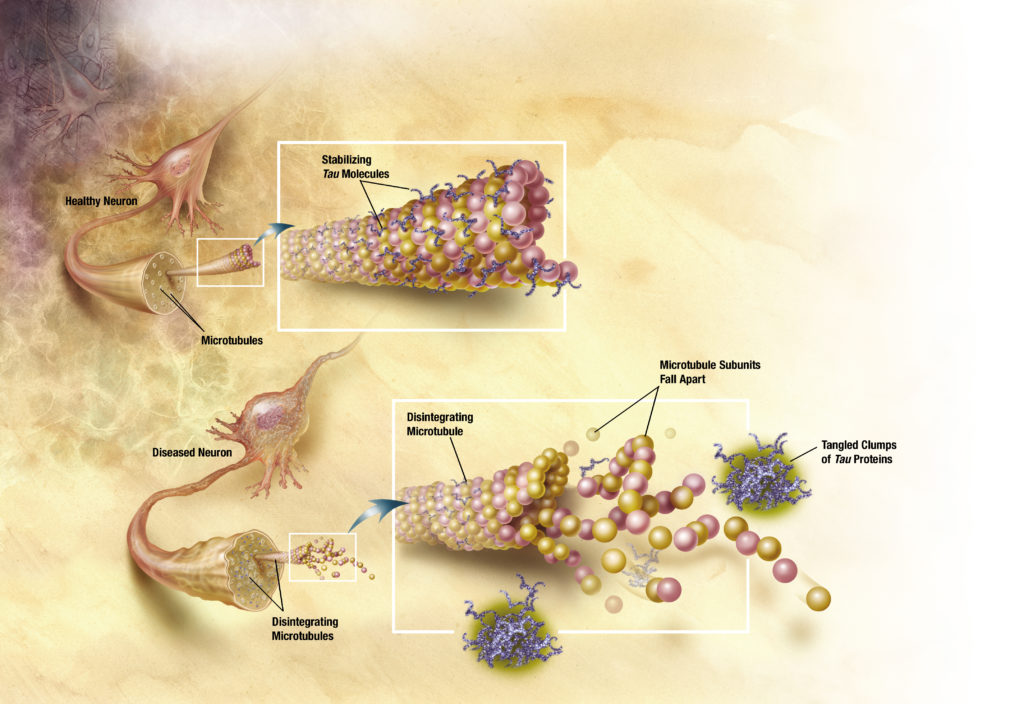
Courtesy of ADEAR: “Alzheimer’s Disease Education and Referral Center, a service of the National Institute on Aging.”
I ricercatori che hanno condotto lo studio, guidati da Anthony Fitzpatrick, hanno ipotizzato che le modifiche post-traduzionali, ovvero quelle variazioni che la proteina subisce sulla sua superficie, abbiano un ruolo attivo nel malfunzionamento di tau. L’obiettivo è identificare con precisione la struttura della proteina in tessuti cerebrali di pazienti affetti da due diverse taupatie: la degenerazione corticobasale, malattia imputabile interamente a tau, e il morbo di Alzheimer, in cui sembra che la proteina sia implicata sia nell’esordio che nella progressione della malattia. Gli scienziati hanno dovuto aggirare un duplice ostacolo: l’enorme piccolezza delle fibre proteiche (diecimila volte più sottili di un capello) e la complessità chimica delle modifiche post-traduzionali. Per riuscire nel loro intento, hanno combinato una tecnica di microscopia, la criomicroscopia elettronica, con una analitica, la spettrometria di massa.
La criomicroscopia, sviluppata in parte proprio alla Columbia University e che è valsa, nel 2017, il premio Nobel per la chimica a Jacques Dubochet, Joachim Frank e Richard Henderson, consente di osservare in dettaglio molecole in soluzione, risultando particolarmente vantaggiosa per studiare molecole biologiche come le proteine. Per individuare le modificazioni post-traduzionali, invece, i ricercatori sono ricorsi alla spettrometria di massa, tecnica per la quale nel 2002 John Bennett Fenn e Kōichi Tanaka sono stati insigniti del premio Nobel per la chimica: questa permette di individuare la composizione chimica di sostanze separandole in base al loro rapporto tra massa e carica.
La combinazione delle tecniche ha permesso di capire che le modifiche sulla superficie di tau influenzano la struttura delle fibre e determinano differenze significative non solo tra le varie taupatie, ma anche tra i singoli pazienti: una visione della proteina in alta definizione che può fornire informazioni utili per la diagnosi precoce di queste malattie, oltre a offrire potenziali target di farmaci futuri. “Le nostre scoperte ispireranno nuovi approcci per lo sviluppo di strumenti diagnostici e la progettazione di farmaci per rallentare la progressione della malattia”, afferma Fitzpatrick. “Le malattie neurodegenerative sono tra le classi di malattie più complesse e angoscianti, ma attraverso il nostro lavoro e quello dei nostri colleghi e collaboratori, stiamo costruendo una tabella di marcia verso diagnosi e terapie efficaci”. Verso un futuro in cui sarà più semplice, è il caso di dirlo, vederci chiaro sulle malattie neurodegenerative.
Immagine in evidenza: National Institute on Aging, NIH





















Commenti recenti